fenylalanin är en proteinogen, essentiell aminosyra med en aromatisk sexledad ring som fungerar som en byggsten för många proteiner och peptider.
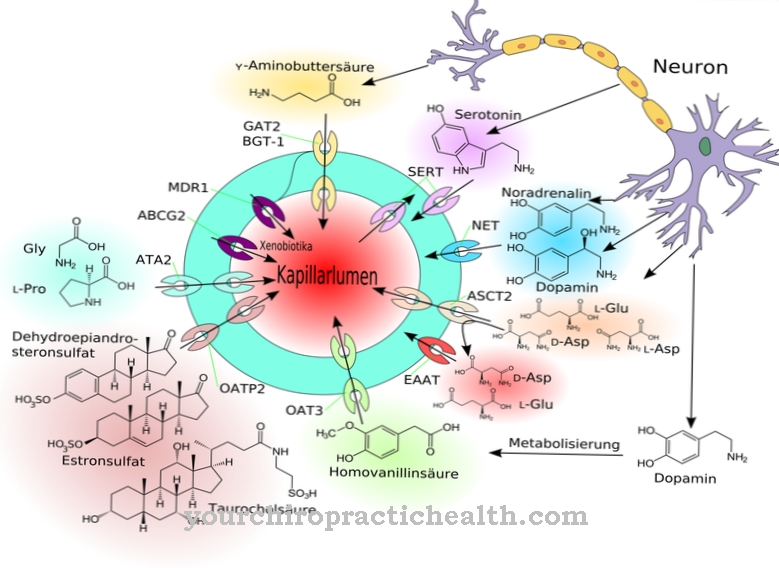
Dessutom spelar fenylalanin en viktig roll i kvävemetabolismen och kan omvandlas i levern till den proteinogena aminosyran tyrosin. Fenylalanin och tyrosin spelar en viktig roll i syntesen av insulin, melanin, tyroxin och neurotransmittorer dopamin, serotonin och tyramin.
Vad är fenylalanin?
Fenylalanin är en essentiell alfa-aminosyra som - till skillnad från de flesta proteinogena aminosyror - inte bara är bioaktiv i L-formen, men i begränsad utsträckning också som en enantiomer i R-formen.
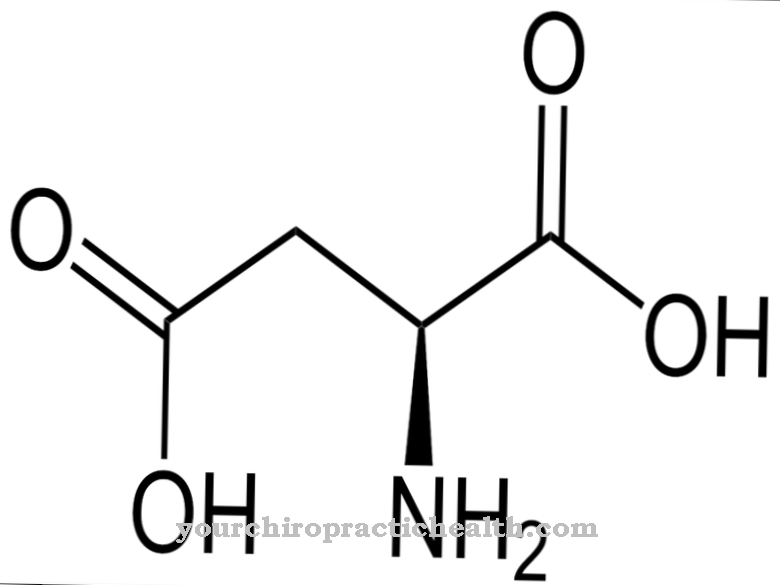
R-fenylalanin är biokemiskt till stor del inaktivt och sker uteslutande i den konstgjorda produktionen av aminosyran, men rollen för D-fenylalanin i kontrollen av vissa neurotransmittorer inom smärtkomplexet diskuteras. Som ett karakteristiskt strukturellt drag har fenylalanin en enkel aromatisk sex-ledad ring (bensenring) med en bifogad kolvätekedja. Den kemiska strukturformeln är C6H5-CH2-CH (NH2) -COOH, varvid C6H5-gruppen indikerar bensenringen. Aminosyran är amfifil, vilket innebär att den är både fett och vattenlöslig.
Den kemiska formeln visar också att fenylalanin uteslutande består av kol, väte, kväve och syre, ämnen som är allestädes närvarande. Sällsynta metaller, mineraler eller spårämnen ingår inte i aminosyran. Ändå kan den mänskliga metabolismen inte syntetisera fenylalanin i tillräcklig grad från tyrosin, men är beroende av intag från mat. Fenylalanin finns i tillräckliga mängder i många djur- och grönsaksmat, så att med en normal, blandad diet - under förutsättning att matsmältningskanalen normalt absorberas - finns det ingen anledning att frukta en brist på aminosyran.
Funktion, effekt och uppgifter
Fenylalanins viktigaste funktion och uppgift är att delta i strukturen för många proteiner och peptider. Det är också involverat i syntesen av vissa hormoner som spelar en central roll i kontrollen av metaboliska processer.
Det är hormoner som adrenalin, noradrenalin, L-dopa, PEA och melanin. Dessutom tjänar L-fenylalanin som den basiska substansen från vilken z. B. budbärarämnet dopamin, serotonin, tyramin och andra kan syntetiseras. L-fenylalanin tjänar också som utgångsmaterial för den essentiella aminosyran tyrosin. För detta ändamål omvandlas fenylalanin till tyrosin i levern i två steg genom hydroxylering och genom uppdelning av en vattenmolekyl. Fenylalaninhydroxylas är det enzym som katalyserar omvandlingen till tyrosin.
En alternativ tillförsel av den också essentiella aminosyran tyrosinburk - som med fenylalanin - sker genom matintag. Till skillnad från alla andra aminosyror, som bara har en bioaktiv effekt i sin L-form, verkar D-enantiomeren av fenylalanin åtminstone påverka uppfattningen av smärta. En blandning av L- och D-fenylalanin (racemisk blandning) befanns ha en smärtstillande effekt. DL-blandningen blockerar sannolikt nedbrytningen av enkefaliner - kroppens egna opioider - så att den smärtstillande effekten förlängs och intensifieras.
Utbildning, förekomst, egenskaper och optimala värden
Den essentiella aminosyran fenylalanin absorberas genom mat. Det är inte fritt, men vanligtvis som en del av ett protein eller polypeptid i kemiskt bunden form. För att göra aminosyran tillgänglig för metabolismen måste motsvarande protein först brytas ned under matsmältningsförloppet och sedan extraheras från "fragmenten" med användning av ytterligare enzymer i den ytterligare metabolismen.
L-fenylalanin syntetiseras via den så kallade shikiminsyravägen. Det är en komplex biokatalytisk kedjereaktion som autotrofiska växter och bakterier har. Det speciella med autotrofiska organismer är deras förmåga att bilda organiskt material från enbart oorganiskt material. Gratis L-fenylalanin smakar bittert, medan dess D-enantiomer, som uteslutande produceras i industriell produktion, har en sötaktig smak. Aminosyran är z. B. erbjuds som kosttillskott och ingår också i det artificiella sötningsmedlet aspartam. Biotillgänglig L-fenylalanin finns i bunden form i många livsmedel.
Deras innehåll är särskilt högt i torkade ärtor och sojabönor, i valnötter och pumpafrön samt i olika typer av fisk och kött. Fenylalaninbehovet är starkt beroende av tillförseln av tyrosin. Om det inte finns något tyrosin i kosten behöver kroppen 38 till 52 mg per kg kroppsvikt. Med ett rikt utbud av tyrosin i kosten sjunker det dagliga behovet till endast 9 mg per kg kroppsvikt. Som regel innehåller livsmedel som innehåller fenylalanin också en motsvarande mängd tyrosin.
Rekommendationen från FAO / WHO från 1985 motsvarar ett kombinerat krav på L-fenylalanin och L-tyrosin om 14 mg per kg kroppsvikt per dag. En vuxen med en kroppsvikt på 80 kg behöver därför 1 120 mg av båda ämnena per dag.
Sjukdomar och störningar
Symtom på brist när det finns ett permanent otillräckligt utbud av fenylalanin och tyrosin i kosten är extremt sällsynta, men kan få allvarliga konsekvenser, särskilt i neuronområdet.
Bortsett från en nedsättning av syntesen av många hormoner och neurotransmittorer, kan bristen också indikeras av en störning i myeliniseringen av nervfibrer. Det motsatta av en brist, en överkoncentration av fenylalanin (fenylketonuria), kan uppstå på grund av en genetisk metabolisk störning. Sjukdomen ärvs på ett autosomalt recessivt sätt och leder till en reducerad produktion av enzymet fenylalaninhydroxylas, vilket kan omvandla fenylalanin till tyrosin.
Den reducerade enzymaktiviteten leder till en kraftig ökning av aminosyran, till vad som kallas fenylketonuri, eftersom omvandlingen till tyrosin också är nedbrytningsvägen för fenylalanin. Samtidigt saknas tyrosin eftersom syntesvägen är blockerad. En annan ärftlig sjukdom i detta sammanhang är Hartnup-syndrom. Det är en metabolisk störning som stör störningen av fenyalanin över cellmembranet. Detta leder till allvarliga problem i CNS, på huden och i matsmältningskanalen.


.jpg)